مقدمه
پیشرفتهایی که در سده اخیر نصیب علم ژنتیک شده است، تا حدود زیادی مرهون مطالعه و بررسی وراثت در باکتریها است. امروزه ثابت شده است که مکانیسمها ژنتیکی در باکتریها از نظر واکنشهای شیمیایی مشابه یاختههای یوکاریوت است. پروکاریوتها موجودات ساده و مناسبی برای بررسیهای ژنتیکی هستند. زیرا در آنها تنها یک مولکول DNA در هر یاخته وجود دارد و این DNA دارای ساختار کروموزمی پیچیدهای نیست. استفاده از میکروارگانیسمها به عنوان ابزار مطالعه ژنتیکی دارای نقاط ضعفی نیز است.
اول آنکه کوچکی اندازه این موجودات بررسی ویژگیهای ظاهری هر یاخته را دشوار میسازد. دوم آنکه تولید مثل جنسی در این موجودات وجود ندارد و یا بطور ناقص دیده میشود. پس از اینکه ساختار مولکولی DNA که نخستین بار بوسیله واتسون و کریک معرفی و ارائه شد، نحوه بیوسنتز آن را نیز در یاخته مشخص کردند. در اواخر سالهای 1950 ، کریک اصل بنیادی را مطرح کرد. این اصل بیان کننده چگونگی انتقال اطلاعات ژنتیکی از مولکول DNA به RNA و ترجمه آن در پروتئینها است.
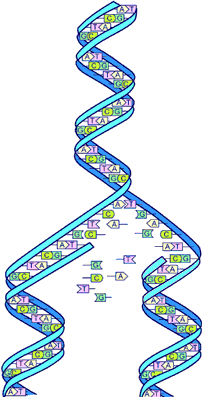 |
همانندسازی DNA
در مطالعات اولیه برای همانندسازی سه الگو مطرح شد که شامل الگوهای حفاظتی ، نیمه حفاظتی و پراکنده است. در الگوی حفاظتی از روی مارپیچ دو رشتهای DNA ، یک مولکول کامل DNA ساخته میشود. در الگوی نیمه حفاظتی ابتدا دو رشته DNA از هم باز شده و در مقابل هر یک از رشتهها ، رشته مکمل ساخته میشود. در الگوی پراکنده ابتدا مولکول DNA به قطعاتی تقسیم میگردد و هر یک از قطعه رشته مکمل خود را سنتز میکند. واتسون و کریک با پژوهشهای خود بر روی مولکول DNA ، الگوی نیمه حفاظتی را منطقی و تنها راه همانند سازی میدانستند. سپس مزلسون و استال با انجام آزمایشهای بسیار ظریف و مهم ، درستی چنین الگویی را به اثبات رساندند.
آزمایش مزلسون و استال
مزلسون و استال برای اثبات فرآیند همانند سازی آزمایشی انجام دادند که به شرح زیر میباشد. آنها ابتدا یاختههای باکتری اشرشیاکلی را در محیط کشت ویژهای که نیتروژن آن از نوع سنگین (N15) بود، برای زمان معین کشت دادند و سپس یاختهها را به محیط کشت عادی که نیتروژن آن از نوع سبک (N14) بود، انتقال دادند و در محدودههای زمانی معین از یاختههای نسلهای اول ، دوم و سوم حاصل از محیط کشت جدید ، نمونه برداری کرده و DNA آنها را به روشهای اختصاصی جدا ساختند. نمونههای DNA بر روی گرادیان (شیب) چگالی کلرور منیزیم سانتریفوژ شده و در این روش ترکیبات مختلف بر اساس چگالی آنها جدا سازی میشوند.
بدین ترتیب DNA واجد وزنهای متفاوت از یکدیگر جدا میشوند. DNA معمولی که N14 دارد (DNA سبک) به علت داشتن چگالی کمتر در بالای لوله قرار میگیرد. در حالی که مولکول DNA با (N15 سنگین) در محلی پایین تر از DNA سبک واقع میشود. DNA های واجد مقادیر متفاوت N15 و N14 نیز در بینابین این دو حد جای میگیرند.
با کشت یاختههای دارای DNA واجد نیتروژن سنگین در محیط کشت حاوی نیتروژن سبک مشاهده میشود که مولکول DNA ماهیت سبک - سنگین پیدا میکند. یعنی دو رشته DNA کاملا از هم باز شده و رشتههایی در تکمیل هر یک از دو رشته قبل ساخته میشود. این رشتههای جدید همگی دارای نیتروژن سبک (محیط کشت جدید) هستند. با ادامه کشت در نسلهای دوم و سوم ملاحظه میشود که از میزان DNA سبک - سنگین کم شده و به DNA سبک افزوده میشود.
نتیجه آزمایش مزلسون و استال
مزلسون و استال با چنین مشاهداتی نتیجه گرفتند که همانند سازی در مولکول DNA به طریق نیمه حفاظتی صورت میگیرد که مستلزم باز شدن دو رشته از هم و سنتز مولکول DNA جدید در مقابل هر رشته قدیم است. این پدیده به نام همانند سازی مشهور است.
آنزیمهای لازم در همانند سازی
آنزیمهای پلیمراز
آنزیمهایی هستند که پلیمر شدن زنجیرههای پلینوکلئوتیدی را کاتالیز میکنند. تا کنون سه نوع آنزیم پلیمراز به نامهای Ι و ΙΙ و ΙΙΙ جداسازی و مشخصات آنها ارائه شدهاند. از بین آنها آنزیم پلیمراز ΙΙΙ نقش اصلی را در سنتز DNA دارد. از خصوصیات مهم آن ، این است که منحصرا نوکلئوتیدها را در جهت '5 به '3 بهم متصل میکنند و در جهت عکس نمیتواند عمل کند. آنزیم پلیمراز ΙΙ نیز در مرحلهای از سنتز DNA وارد شده و سنتز را در جهت '3 به '5 پیش میبرد. و آنزیم پلیمراز I عمل ترمیم همانند سازی را انجام میدهد.
آنزیم هلیکاز
این آنزیم به مولکول DNA دو رشتهای متصل شده و با عمل خود موجب باز شدن دو رشته از یکدیگر میشود.
آنزیم لیگاز
در مرحلهای از سنتز DNA وارد عمل شده و دو رشته DNA را بهم پیوند میدهد.
آنزیم پریماز
آنزیمی است که در ساختن قطعه کوچک RNA پرایمر ، هنگام همانند سازی وارد عمل شده و نوکلئوتیدهایی از نوع اسید ریبونوکلئوتید را به یکدیگر متصل میکند. تعدادی پروتئینهای ویژه وجود دارند که پس از باز شدن دو رشته DNA از یکدیگر به محلهای باز شده متصل شده و مانع اتصال مجدد دو رشته به یکدیگر میشوند.
 |
همانند سازی متوالی
در روی مولکول DNA نقاطی وجود دارند که همانند سازی از آنها آغاز میشود. این نقاط مبدا همانند سازی خوانده میشوند. در DNA باکتریها ، یک مبدا همانند سازی و در DNA موجودات عالی ، تعدادی زیادی از این مبدا وجود دارند. هنگام همانند سازی ابتدا آنزیم هلیکاز به مارپیچ دو رشتهای DNA متصل شده و پیچش DNA را در آن نقطه باز میکند. پرتئینهای DBP به ناحیه باز شده هجوم آورده و با اتصال به DNA تک رشتهای مانع از جفت شدن بعدی DNA میشوند.
ناحیهای را که هلیکاز به آن متصل میشود، چنگال همانند سازی مینامند. همانند سازی به صورت دو سویه است. آنزیم پلیمراز ΙΙΙ که اتصال نوکلئوتیدها را به یکدیگر به عهده دارد، فقط میتواند همانند سازی را در جهت 3 به 5 پیش ببرد. در این حالت دو رشته مولکول DNA در خلاف جهت یکدیگر هستند. در نتیحه رشتهای که در جهت '5 به '3 سنتز میشود، به راحتی سنتز DNA را آغاز کرده و پیش میبرد. این رشته به نام رشته راهنما معروف است. در همانند سازی این رشته را متوالی مینامند.
همانند سازی نامتوالی
در مولکول DNA رشتهای که '5 آزاد دارد، سنتز DNA طبق آنچه درباره رشته راهنما ذکر شد، انجام نمیگیرد. دلیل آن این است که آنزیم پلیمراز ΙΙΙ نمیتواند نوکلئوتیدها را در جهت 3 به 5 کاتالیز کند. لذا میبایست مکانیسم دیگری برای سنتز این رشته از DNA وجود داشته باشد. این رشته DNA به نام رشته عمل کننده یا پیرو معروف است. در این حالت ابتدا دو رشته DNA در فواصل معینی از یکدیگر باز شده و آنزیم پریماز در آن محل قرار میگیرد و با استفاده از ریبونوکلئوتیدها ، RNA کوچکی ساخته میشود که RNA پرایمر نام دارد.
انتهای 3 این RNA کوچک که از روی الگوی DNA ساخته شده است، میتواند به آنزیم پلیمراز III امکان دهد تا دزاکسی ریبونوکلئوتیدها را به انتهای آن متصل کند. لذا در این رشته از مولکول DNA قطعاتی از DNA سنتز میشوند که قطعات اوکازاکی نام دارد. (اوکازاکی نخستین کسی بود که این قطعات سنتز شده DNA را با میکروسکوپ الکترونی مشاهده کرد).
در این حالت آنزیم پلیمراز I وارد عمل شده و به ترتیب یکی یکی ریبونوکلئوتیدها را در جهت 5 به 3 برداشته و به جای آنها نوکلئوتیدهای از انواع دزاکسی جایگزین میکند تا این که قطعات همه از نوع دزاوکسی شوند. سپس انتهای قطعات ساخته شده بوسیله آنزیم لیگاز به هم متصل شده و یک رشته ممتد DNA حاصل میشود. اندازه هر قطعه اوکازاکی حدود 1000 تا 2000 نوکلئوتید است.